|
Вода составляет 60- 75% организма (медуза -98%), является основой внутренней среды организма. Для гидробионтов она еще является и внешней средой.
Вода бывает:
- Связанная (4-5%) - входит в состав клеточных структур → образует пленку вокруг белков, предотвращая их растворение.
- Свободная (95-96%) - не связана с другими соединениями (основа крови, лимфы, межклеточной жидкости)
Структура воды:
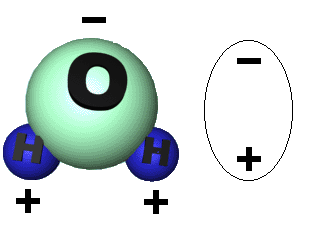 Вода состоит из 1 атома оксигена и 2 атомов гидрогена, соединенных прочной ковалентной связью. Молекула воды - диполь. Благодаря этому 2 молекулы воды притягиваются за счет сил электростатического взаимодействия между разноименными зарядами, образуется непрочная водородная связь (в 25 раз слабее ковалентной) ⇒ обычное агрегатное состояние воды жидкость ( при температуре 0-100оС). При изменении температуры агрегатное состояние может изменятся: <0о С - твердое (лед), >100о С - газообразное (водяной пар). Вода состоит из 1 атома оксигена и 2 атомов гидрогена, соединенных прочной ковалентной связью. Молекула воды - диполь. Благодаря этому 2 молекулы воды притягиваются за счет сил электростатического взаимодействия между разноименными зарядами, образуется непрочная водородная связь (в 25 раз слабее ковалентной) ⇒ обычное агрегатное состояние воды жидкость ( при температуре 0-100оС). При изменении температуры агрегатное состояние может изменятся: <0о С - твердое (лед), >100о С - газообразное (водяной пар).
Свойства и функции воды:
1. Превосходный растворитель (для полярных соединений).
Вещества: а) Гидрофильные - растворимые в воде (поваренная соль, глюкоза, сахароза, простые белки и др.)
б) Гидрофобные - нерастворимые в воде ( липиды, сложные белки и углеводы и др.)
Вода как универсальный растворитель играет важную роль в обмене веществ, транспорте различных соединений по организму...
2. Большая теплоемкость. Это защищает организм от резкого снижения температуры тела и перегрева, а также обеспечивает протекание биохимических реакций.
3. Большая теплопроводность. Вода равномерно распределяет тепло по всему организму.
4. Высокая теплота испарения. Это способствует охлаждению тела.
5. Упругость молекул. Благодаря этому создается тургорное давление, которое определяет объем и упругость клеток и тканей.
Максимальная плотность воды наблюдается при температуре +4оС.
6. Большое поверхностное натяжение за счет слипания молекул (коггезия). Молекулы воды могут слипаться с молекулами других веществ (адгезия). Это обеспечивает капиллярный кровоток, восходящие и нисходящие токи воды в растворах, движение по капиллярам деревьев против гравитационных сил.
7. Способность к ионизации. Н2О ⇔Н+ + ОН-. От концентрации Н+ зависит рН среды. Нейтральная реакция - рН 7,0. Если значение ниже - кислая реакция, если выше - щелочная.
8. Принимает участие в реакция расщепления. Гидролиз - химическая реакция взаимодействия вещества с водой, при которой происходит разложение этого вещества и воды с образованием новых соединений.
Водный баланс - равновесие между количеством поступившей в организм воды и тем, что выделяется.
При потере ⇒2% - жажда, 12% - смерть.
Презентация Вода скачать
|